2026年3月9日,亚娱体育app官网下载(2696.HK)宣布,基于自主研发的创新型T细胞衔接器(T-cell engager, TCE)平台开发的创新分子——HLX3901(DLL3 x DLL3 x CD3 x CD28 四特异性抗体)的新药临床试验(IND)申请已获得国家药品监督管理局(NMPA)批准,拟用于晚期或转移性实体瘤的治疗,有望为临床难治性肿瘤,如小细胞肺癌(SCLC)等神经内分泌癌(NEC)带来突破性的免疫治疗方案。
Delta样配体3(Delta-like ligand 3,DLL3)是一种抑制性Notch配体1-2,在约80%的小细胞肺癌(SCLC),及其他神经内分泌癌中高表达3-5,在正常组织中表达水平极低6-7。DLL3的高度特异性表达使其成为SCLC治疗的理想靶点,以T细胞衔接器(TCE)为代表的精准免疫治疗正成为最具前景的研究方向。目前,已有靶向DLL3及CD3的TCE双特异性抗体获批上市8,并展现出良好的治疗潜力9,但肿瘤微环境(TME)中的T细胞浸润不足和免疫抑制状态仍然是限制TCE疗效的关键瓶颈10-11,单纯的CD3激活信号(第一信号)在缺乏共刺激信号(第二信号)的情况下,易导致T细胞失能12,无法实现持久、深入的抗肿瘤疗效。CD28是表达于T细胞表面的关键共刺激分子,其通过与抗原呈递细胞(APC)表面的配体CD80(B7-1)和CD86(B7-2)结合,提供T细胞活化的第二信号,对T细胞的完全活化极为关键13-14。
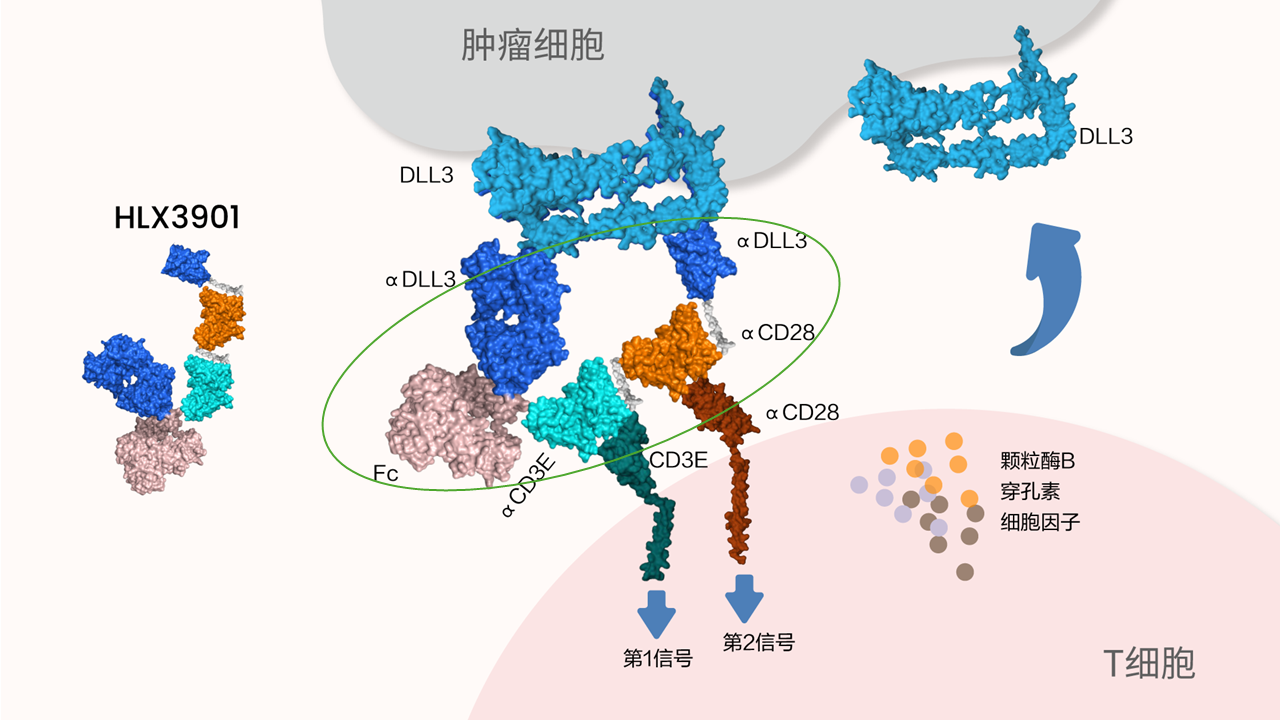
HLX3901是一款拥有自主知识产权的四特异性抗体药物,能够精准靶向DLL3双表位、CD3和CD28,作为新一代T细胞衔接器,HLX3901旨在增强对肿瘤细胞的杀伤,克服免疫抑制,并优化T细胞衔接器在实体瘤中的治疗窗口。其作用机制主要包括:
1)通过同时结合T细胞表面的CD3(第一信号) 和CD28 (共刺激信号),实现对T细胞的双重激活,从而增强T 细胞对DLL3阳性肿瘤细胞的靶向杀伤能力,提升抗肿瘤疗效;
2)通过协同激活T细胞第一信号与共刺激信号,促进T细胞的活化、增殖和存活能力,进而延长抗肿瘤免疫应答的持续时间,在低T细胞浸润的条件下依然展现出优异的抗肿瘤活性。
临床前研究显示,HLX3901在低效靶比条件下展现出更优的细胞毒性效应。在人类泛T细胞重构模型中,HLX3901比同类产品(如Tarlatamab)表现出更强且更持久的抗肿瘤活性。同时,在食蟹猴的初步毒性研究中,HLX3901耐受性良好,显示出较宽的治疗窗口。
作为亚娱体育app官网下载在免疫细胞衔接器领域的重要布局,HLX3901结合了公司AI驱动的智能药物设计与TCE平台技术,通过精巧的分子设计,该产品兼具持久的特异性T细胞激活、攻克低T细胞浸润肿瘤及显著降低细胞因子释放综合征(CRS)等多重优势,旨在克服第一代TCE在实体瘤治疗中的主要障碍。目前,公司已搭建起包括PD(L)1为核心的免疫检查点抑制剂平台、免疫细胞衔接器平台(如多特异性TCE平台)、Hanjugator™ADC 平台、AI驱动的一站式早期研发平台HAI Club在内的多维创新平台矩阵,在保障单个项目的研发质量与效率的同时,为打造具备全球竞争力的中长期创新管线提供了可持续的系统能力支撑。
深耕未满足的临床需求,公司加速扩充由高潜力分子组成的早期管线储备,多款产品于近期取得里程碑进展,HLX37(创新抗PD-L1/VEGF双特异性抗体)已获得IND批准用于晚期实体瘤治疗并高效完成首例患者给药;HLX701(新型SIRPα-Fc融合蛋白)凭借潜在更优的安全性,已启动在国内的II期临床研究,HLX97(新型KAT6A/B口服小分子抑制剂)也于近期同步获得CDE新药临床试验许可;更多临床前候选分子如HLX3902(STEAP1xCD3xCD28三特异性TCE)、HLX49(HER2双表位ADC)、HLX48(EGFRxcMET双抗ADC)、HLX105(一款抗体融合蛋白)在内的多个前沿分子也将加速迈向临床,为公司创新管线不断注入新鲜血液。
未来,亚娱体育app官网下载将继续坚持“以患者为中心”的研发理念,依托平台化、系统化的创新体系,加速推进具有全球竞争力的差异化创新管线布局,为全球患者提供更可及、更有效的治疗选择。
【参考文献】
1.Kim JW, et al. DLL3 regulates Notch signaling in small cell lung cancer. iScience. 2022;25(12):105603.
2.Ladi E, et al. The divergent DSL ligand Dll3 does not activate Notch signaling but cell autonomously attenuates signaling induced by other DSL ligands. J Cell Biol. 2005;170(6):983-992.
3.Owen DH, et al. DLL3: an emerging target in small cell lung cancer. J Hematol Oncol. 2019;12(1):61.
4.Tanaka K, et al. Prevalence of Delta-like protein 3 expression in patients with small cell lung cancer. Lung Cancer. 2018;115:116–120.
5.Yao J, et al. DLL3 as an Emerging Target for the Treatment of Neuroendocrine Neoplasms. Oncologist. 2022 Nov 3;27(11):940-951.
6.Rudin CM, et al. Emerging therapies targeting the delta-like ligand 3 (DLL3) in small cell lung cancer. J Hematol Oncol. 2023;16(1):66.
7.Lobenhofer E, et al. P1.12-18 Nonclinical Safety Assessment of AMG 757, a DLL3 Bispecific T Cell Engager, in the Cynomolgus Monkey. Journal of Thoracic Oncology. 2019;14(10):S541.
8.Dhillon S. Tarlatamab: First Approval. Drugs. 2024;84(8):995-1003.
9.Ahn MJ, et al. Tarlatamab for Patients with Previously Treated Small-Cell Lung Cancer. N Engl J Med. 2023;389(22):2063-2075.
10.Hegde PS, Chen DS. Top 10 Challenges in Cancer Immunotherapy. Immunity.2020;52(1):17-35.
11.Belmontes B, et al. Immunotherapy combinations overcome resistance to bispecific T cell engager treatment in T cell-cold solid tumors. Sci Transl Med. 2021;13(608): eabd1524.
12.Schwartz RH. T cell anergy. Annu Rev Immunol. 2003;21:305-334.
13.Esensten JH, et al. CD28 Costimulation: From Mechanism to Therapy. Immunity. 2016;44(5):973-988.
14.Bhatia S, et al. Different cell surface oligomeric states of B7-1 and B7-2: implications for signaling. Proc Natl Acad Sci U S A. 2005;102(43):15569-15574.